Ⅰ. Introduction
근거중심의료의 개념이 확산되면서 임상연구의 중요성이 부각되고 있다1). 임상연구는 일반적으로 관찰 연구 (observational study)와 중재연구 (interventional study)로 나뉜다2). 중재연구는 연구자가 연구 전반의 어느 시점에서 개입하게 되며, 질병에 대한 치료나 예방적인 조치의 직접적인 영향을 평가하기 위해서 사용된다3).
소아를 대상으로 한 중재연구는 성인에 비해 그 수도 매우 적으며, 연구 대상도 특정 질환에 치우쳐 있는 실정이다4). 소아는 윤리적, 안전성 문제로 인해 시판 전 임상시험에서 제외되는 경우가 많고, 대부분의 약제들은 성인을 기준으로 개발되어 소아에게 그 연령에 허가되지 않은 약품 (off-label)이 투여되는 경우가 많다5) . 소아 대상 중재연구의 부족으로 성인 대상 연구결과를 기반으로 추론하여 소아에 적용하고 있지만, 소아의 질환이나 약물 대사능력이 성인과는 다르기 때문에 약물유해반응의 위험이 높다6). 따라서 소아 대상 중재 연구는 소아에게 유효성과 안전성이 보장된 치료를 시행하는 데 필수적이라고 볼 수 있다7).
한의계 내에서도 한의학의 효과를 객관적으로 증명하려는 임상시험에 대한 관심이 높아지고 있으며 임상연구 또한 증가하고 있는 추세이다8). 하지만 아직까지 국내에서 소아청소년 대상 한의 중재연구는 많이 부족한 상황이다. 체질 개선과 근본적인 치료를 원하는 소아 환자들이 증가함에 따라 소아 한방치료에 대한 관심이 고조되고 있으나9) 부모 대상 한방치료에 대한 인식 조사 결과, 한방 진료 시 걱정되는 점으로 한약의 유해물질이나 부작용 같은 안전성에 대한 염려가 높은 비중을 차지하는 것으로 나타났다10).
소아 한방치료의 유효성과 안전성을 확인하는 중재 연구는 소아 한방치료의 대중화를 위해서 한방소아과 영역의 중요한 과제가 될 것이다. 한방 소아 중재연구를 본격적으로 시행하기에 앞서 현재까지 시행된 소아 중재연구의 특성을 파악하고 이해하는 것이 필요할 것으로 여겨진다. 한방소아과 분야에서는 중의학 논문을 중심으로 한 임상연구 동향에 대한 연구11-13), 천식에 대한 국외 임상연구 동향에 대한 연구14), 특정 질환에 대한 국내 임상연구 동향에 대한 연구15), 한방소아과학회지에 출판된 임상연구 논문에 대한 분석 연구16)는 있었으나 국내에서 시행된 소아청소년 대상 중재 임상연구에 대한 동향은 아직까지 보고되지 않았다
전세계적으로 임상연구의 출판 치우침 (publication bias)을 막고 임상연구의 윤리적 수행을 위해 임상시험 사전 등록의 필요성이 제기되어 왔으며, 국내에서도 질병관리본부 국립보건연구원에서 운영하는 임상연구 정보서비스 (Clinical Research Information Service, CRIS)가 2010년 5월부터 시행되어 임상시험 등록을 권고하고 있다1). 이에 본 저자는 CRIS 등록부를 통해 기존에 국내에서 소아청소년 대상 어떤 중재 임상연구가 계획 및 등록되어 있는지 조사하고, 한의 중재연구 현황을 파악하여 향후 소아청소년 대상 한의 중재연구를 위한 기초자료로 활용하고자 본 연구를 수행하였다.
Ⅱ. Material and Methods
1. 대상 연구 검색 및 선정
CRIS에 등록된 임상시험을 대상으로 검색하였다. 국내에서 CRIS가 구축된 2010년 5월부터 검색일 이전까지 등록된 모든 임상연구를 검색하였으며, 2018년 10월 12일 검색을 실시하였다.
검색어로는 ‘소아’, ‘아동’, ‘청소년’, ‘영아’, ‘유아’, ‘초등학생’, ‘중고등’, ‘중학생’, ‘고등학생’을 사용하였다. 이후 검색된 임상연구 중 소아청소년을 대상으로 시행된 치료 또는 보조적 치료를 목적으로 한 중재연구만을 포함하였다. 검색된 연구의 제목 및 원문을 읽어보고 소아청소년 대상이 아닌 연구나 관찰연구, 중재연구 중 치료나 보조적 치료가 목적이 아닌 연구들은 최종 분석 대상에서 제외시켰다.
2. 자료추출
선정된 임상연구에서 CRIS에 등록된 연도, 중재종류, 연구대상, 연구책임기관, 모집현황, 시험단계, 사전 동의서 작성 유무, 안전성 조사 유무, 보상 여부 등을 중심으로 자료를 추출하였다. 그 중 연구대상에서는 연구대상자 수, 연령, 상태 및 질환, 포함 기준 및 제외기준에 대한 정보를 추출하였다.
Ⅲ. Results
1. 임상연구 검색 및 선정 결과
CRIS에서 2010년 5월부터 2018년 10월까지 소아청소년 임상연구를 검색한 결과 총 112편의 임상연구가 검색되었다. 연구자가 제목 및 내용을 검토하여 소아청소년 대상이 아닌 연구 1편, 관찰연구 34편을 제외하였다. 총 77편의 중재연구 중 연구 목적이 예방인 연구 10편, 진단인 연구 4편, 기초과학인 연구 10편, 기타 16편으로 총 40편을 제외하여 최종적으로 치료 또는 보조적 치료를 목적으로 한 중재연구 37편을 선정하였다 (Fig. 1).
Fig. 1. Flow diagram of interventional study searching and selection
2. 포함된 임상연구의 특성
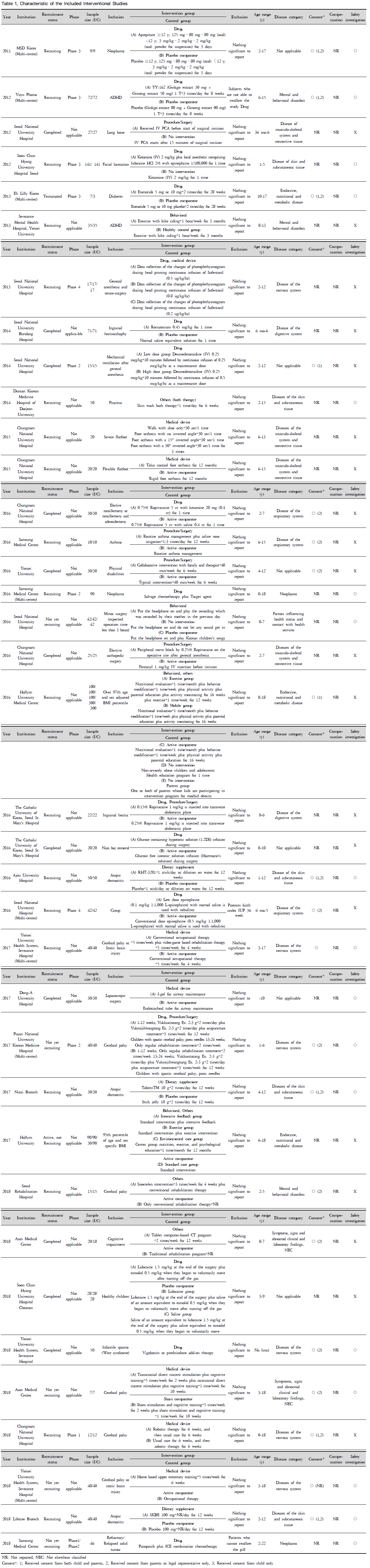
선정된 37편의 중재연구의 CRIS에 등록된 연도, 중재종류, 연구대상, 연구책임기관, 모집현황, 시험단계, 사전 동의서 작성 유무, 보상 여부, 안전성 조사 유무 등의 특성은 다음과 같다 (Table 1).
Table 1. Characteristic of the Included Interventional Studies
 1) 연도별 등록현황
1) 연도별 등록현황
선정된 중재연구를 등록된 연도별로 분류한 결과 (Fig. 2), 2016년에 등록 건수는 11편으로 가장 많았으며, 그 뒤로 2018년 9편, 2017년 5편 순으로 많았다. 연도별 전체 중재연구와 소아청소년 대상 중재연구 수 (치료 외 목적 포함)를 비교해 보았을 때 (Fig. 3), 전체 중재연구 중 소아청소년 대상 중재연구의 비율은 전반적으로 2-6% 정도로 나타났다. 소아청소년 대상 치료목적 중재연구만을 비교했을 땐 전체 중재연구의 0-3.5% 정도를 차지하는 것으로 나타났다.
Fig. 2. Distribution of selected interventional studies by year
Fig. 3. Number of total interventional studies and interventional studies for pediatric patient registered into CRIS from 2011 to 2018
2) 중재종류
선정된 중재연구를 중재종류별로 분류한 결과 의약품 13편 (35.1%), 의료기구 7편 (18.9%), 두 가지 이상의 중재가 혼합되어 있는 경우 5편 (13.5%), 시술/수술 4편 (10.8%), 식이보충제 3편 (8.1%), 기타 3편 (8.1%), 행동요인 2편 (5.4%)으로 나타났다 (Table 2). 두 가지 이상의 중재가 혼합된 경우는 세부적으로 보았을 때 의약품과 의료기구가 혼합된 경우, 의약품과 시술/수술이 혼합된 경우, 행동요인과 기타 중재가 혼합된 경우가 있었다. 한의 중재가 포함된 연구는 총 3편으로 본초추출물, 한약 엑스제 및 침 치료, 한약 입욕제가 사용되었다.
Table 2. Classification of Selected Interventional Studies According to Intervention Type
3) 연구대상질환
선정된 임상연구를 연구대상질환별로 분류한 결과 신경계통 질환 6편 (16.2%), 피부 및 피부 밑 조직 질환 5편 (13.5%), 근육골격계통 및 결합조직 질환 4편 (10.8%), 호흡기계통 질환, 정신 및 행동장애, 내분비 영양 및 대사질환 각각 3편 (8.1%), 신생물, 미분류 증상 징후 임상․검사 이상소견 각각 2편 (5.4%), 건강 상태․보건서비스 영향요인 1편 (2.7%)으로 나타났으며 해당사항 없음은 6편 (16.2%)으로 조사되었다 (Table 3).
Table 3. Classification of Selected Interventional Studies According to Disease Category
4) 모집현황
선정된 임상연구를 모집현황별로 분류한 결과 모집 중이 19편 (51.4%)으로 가장 많았고, 연구종결이 11편 (29.7%), 연구대상자 모집 전 5편 (13.5%), 모집 추가없이 진행 중, 모집 중단 각각 1편 (2.7%) 순이었다 (Table 4). 모집 중단 사유는 연구대상자가 적어 계획된 기간에 연구대상자 모집이 불가하여 중단되었다.
Table 4. Classification of Selected Interventional Studies According to Recruitment Status
5) 임상시험단계
선정된 임상연구를 시험단계에 따라서 분류한 결과, 해당사항 없음이 26편 (70.2%)으로 가장 많았으며, Phase 3이 4편 (10.8%), Phase 2가 3편 (8.1%), Phase 4가 2편 (5.4%), Phase 1, Phase 1/Phase 2가 각각 1편 (2.7%), Phase 2/Phase 3가 0편 순으로 나타났다 (Table 5).
Table 5. Classification of Selected Interventional Studies According to Phase
6) 연구책임기관
선정된 임상연구를 연구책임기관에 따라서 분류한 결과 서울대학교병원과 충남대학교병원이 각각 5편(13.5%)으로 가장 많았으며, 학교법인 연세대학교 의과대학 세브란스병원 및 삼성서울병원이 각각 3편 (8.1%), 학교법인 가톨릭학원 가톨릭대학교 서울성모병원 및 서울아산병원이 각각 2편 (5.4%) 순이었다 (Table 6). 대학이나 대학병원이 주요 등록기관이었으며 일부 임상시험 의뢰기관에서의 등록도 5편 (13.5%) 있었다. 연구책임기관 총 23곳을 지역별로 분류한 결과 서울특별시 소재가 12곳, 광역시 및 세종특별자치시 소재가 4곳, 시 (제주특별자치도 내의 시 포함)소재가 7곳, 군 소재가 0곳으로 나타났다.
Table 6. Classification of Selected Interventional Studies According to Institution
7) 동의
선정된 임상연구를 동의 여부에 따라서 분류한 결과, 동의 여부가 언급되지 않은 연구가 17편 (45.9%)으로 가장 많았으며, 부모나 법정대리인의 동의만 받은 경우가 9편 (24.3%), 부모와 소아 모두 또는 부모나 법정대리인의 동의만 받은 경우가 7편 (18.9%) 순이었다. 부모와 소아 모두에게서 동의를 받은 연구는 2편 (5.4%), 동의는 받았지만 누구에게서 받았는지 명시되지 않은 연구가 2편 (5.4%)으로 그 뒤를 따랐으며 소아의 동의만 받은 연구는 0편이었다 (Table 7).
Table 7 Classification of Selected Interventional Studies According to Whether Consent was Made
Table 8. Classification of Selected Interventional Studies According to Whether Safety was Investigated
8) 보상
선정된 모든 임상연구에서 임상연구에 따른 보상 여부나 보상 내용에 대해서 언급하지 않았다.
9) 안전성 조사 유무
선정된 임상연구를 안전성 조사 유무에 따라 분류한 결과, 안전성을 조사한 연구가 17편 (45.9%), 조사하지 않은 연구가 20편 (54.0%)으로 나타났다 (Table 8).
Table 8. Classification of Selected Interventional Studies According to Whether Safety was Investigated
Ⅳ. Discussion
소아청소년의 한방치료에 대한 관심은 점차 높아지고 있으나, 안전성에 대한 염려가 한방치료 선택에 걸림돌이 되고 있는 것으로 여겨진다10). 한방 소아중재연구의 활성화는 한방소아과 영역의 도전이자 과제이며, 이를 수행하기 위해서는 기존의 연구 동향을 파악하고 이해하는 일이 선행되어야 할 것이다. 이에 저자는 CRIS 등록부를 통해 기존 소아 중재연구의 동향을 파악하고자 하였다.
CRIS를 통해 2010년 5월부터 2018년 10월까지 등록된 임상연구를 대상으로 검색한 결과, 소아청소년 대상 치료목적 중재연구 총 37편이 선정되었다. 선정된 연구들을 연도별로 분석한 결과 2016년에 11편으로 가장 많이 등록되었으며 평균 4.7편이었다. 연도별 전체 중재연구 중 소아청소년 대상 중재연구 (치료목적 외 포함)의 비중은 2-6% 정도로 나타났다. 중재종류별로 분석한 결과 의약품 13편 (35.1%), 의료기구 7편 (18.9%)으로 가장 많았다. 한의 중재가 포함된 연구는 총 3편으로 본초추출물, 한약 엑스제 및 침 치료, 한약 입욕제가 중재로 사용되었다. 연구대상질환별로 분석하였을 땐 신경계통 질환 6편 (16.2%), 피부 및 피부 밑 조직 질환 5편 (13.5%), 근육골격계통 및 결합조직 질환 4편 (10.8%)이 높게 나타났다. 모집현황별로 살펴보면 모집 중이 19편 (51.4%)으로 가장 많았고, 연구종결이 11편 (29.7%), 연구대상자 모집 전이 5편 (13.5%) 으로 그 다음으로 많았다. 임상시험단계별로 살펴보았을 땐 해당사항 없음이 26편 (70.2%)으로 나타났다. 연구책임기관별로 조사하였을 땐 서울대학교병원과 충남대학교병원이 각각 5편을 등록하여 가장 많이 등록한 기관으로 조사되었다. 연구책임기관 총 23곳을 지역별로 나누었을 땐 서울특별시 소재가 12곳으로 과반 이상이 서울 소재인 것으로 나타났다 한방 의료기관은 대전대둔산한방병원, 부산대학교한방병원 총 2곳으로 조사되었다. 동의의 형태나 여부를 조사한 결과 동의 여부가 언급되지 않은 연구가 17편 (45.9%)으로 가장 많았으며, 부모나 법정대리인의 동의만 받은 경우가 9편 (24.3%), 부모와 소아 모두 또는 부모나 법정대리인의 동의만 받은 경우가 7편 (18.9%)으로 다음으로 많았다. 보상에 대해선 모든 연구에서 언급되지 않았다. 안전성을 조사한 연구는 17편 (45.9%), 조사하지 않은 연구는 20편 (54.0%)으로 나타났다.
소아 대상 임상연구는 소아의 건강과 안녕을 향상시키기 위해 필수적이다. 과거에는 성인 대상 연구결과를 추정하여 소아에 사용하였지만, 아이들의 질병 진행이 성인과는 다르고 약물에 대한 반응 또한 연령별로 다르기 때문에 소아 대상 임상연구가 필요한 실정이다17). 하지만 소아 대상 임상연구는 성인 대상 임 상연구보다 시행되기 어렵다. 우선 소아의 의사 결정능력이 연령에 따라 적절하지 않다고 판단되어 동의 절차가 좀 더 복잡하며, 소아를 대상으로 위약을 사용하는 것에 윤리적인 문제가 제기될 수 있고, 연구대상자 모집이 어렵고, 제약사의 투자도 성인보다 적다는 점 등이 소아 대상 임상연구를 어렵게 만든다18).
미국의 경우 BPCA 및 PREA를 시행하여 소아에 대한 임상시험을 반드시 진행하도록 하였고, EU에서도 2006년부터 예외 사항을 제외하고는 소아 임상시험을 반드시 시행하게 하여 off-label을 줄이려는 움직임을 보이고 있으나, 아직 우리나라의 경우 소아 임상시험을 강제하거나 별도의 인센티브를 제공하고 있지는 않다. 따라서 국내 연간 소아 임상시험 건수가 미국이나 EU보다 많이 부족한 상황이다19). 본 연구에서 연도별 CRIS에 등록된 소아 대상 중재연구를 살펴보았을 때 전체 중재연구 중 소아청소년 대상 중재연구가 차지하는 비율이 2-6%로 매우 낮은 것을 확인 할 수 있었고, 최근 3개년 동안 2016년 5.6%, 2017년 3.7%, 2018년 2.6%로 전체 중재연구는 증가하고 있지만 소아청소년 대상 중재연구의 비중은 오히려 감소하는 것으로 나타났다. 이는 박19)의 연구에서 ClinicalTrials.gov에 등록된 국내 소아 임상시험이 전체 임상시험의 10%라고 소개된 것과는 차이가 있는데, 일부 임상연구만이 CRIS에 등록되고 있기 때문이라 사료된다.
중재종류별 분석 결과를 보면 의약품과 의료기구가 많이 사용되었고, 이 외에도 혼합된 중재, 시술/수술, 식이보충제, 행동요인 등이 있었다. 한의 중재는 총 37편의 연구 중 3편의 연구에서 사용되었으며 각각 본초추출물, 한약 엑스제 및 침 치료, 한약 입욕제가 중재로 사용되었다. 이를 통해 한의 중재의 비율이 전체에서 차지하는 비중이 8.1%로 매우 적은 것을 알 수 있었다.
연구대상질환은 신경계통 질환 6편 (16.2%), 피부 및 피부 밑 조직 질환 5편 (13.5%), 근육골격계통 및 결합조직 질환 4편 (10.8%)으로 나타났다. 개별 질환으로 봤을 땐 뇌성마비가 6편으로 가장 많았고 아토피 피부염 3편, 뇌 손상, 비만, 서혜부 탈장, 편평족이 각각 2편으로 그 뒤를 따랐다. 질환에 관계없이 수술 중이나 후에 중재가 시행된 경우는 12편으로, 많은 경우에서 수술적 상황과 동반되어 연구가 시행됨을 알 수 있었다.
최근 임상시험의 사전 등록은 연구윤리적으로 요구되고 있다. 국제의학학술지편집자협의회 (International Committee of Medical Journal Editors, ICMJE)에서는 연구대상자가 연구에 참여하기 전에 임상시험을 사전등록 할 것을 의무화 하였으며, 헬싱키선언에서 또한 첫 연구대상자의 임상시험 등록 이전에 임상시험 등록을 의무화 하는 규정을 추가하였다20). 하지만 본 연구에서 선정된 연구들을 모집현황별로 조사한 결과, 모집 전에 등록된 연구는 총 5편 (13.5%)으로 적게 나타났다. 이에 국내에선 아직 첫 연구대상자 모집 전 임상연구 등록이 미흡함을 알 수 있었다.
임상시험단계는 의약품, 의료기구 또는 생물학적 제제가 인체에 유익하거나 유해한지 결정하기 위한 단계이며, Phase 0, 1, 2, 3, 4가 있다. Phase 0에서는 약역학 및 약물동태가 결정되고 Phase 1에서는 안전성 평가가, Phase 2에서는 유효성 평가가 이루어지고, Phase 3에서 안전성과 유효성을 확증한 뒤 Phase 4에서는 실제 신약이 시판된 후 실제상황에서 신약의 효과와 부작용을 살피게 된다21). 본 연구에서 조사한 결과 해당사항 없음이 26편 (70.2%)으로 매우 높은 비중을 차지하는 것으로 나타났다. 이는 주로 임상시험단계가 의약품을 중재로 사용했을 때 적용되기 때문인 것으로 파악된다. 임상시험단계가 적용된 연구를 살펴보면 Phase 3가 4편 (10.8%), Phase 2가 3편 (8.1%)으로 많은 것을 알 수 있었다. 의약품을 중재로 사용함에도 시험단계가 적용되지 않은 연구가 6편으로 조사되었다. 이 중 5편은 수술적 상황에서 의약품을 사용하는 것으로 조사되었다
가장 많은 소아청소년 대상 중재연구를 등록한 곳은 총 5편을 등록한 서울대학교병원과 충남대학교병원으로 조사되었다. 전반적으론 주로 대학이나 대학병원에서 등록한 것을 알 수 있었고, 일부 임상시험 의뢰기관에서 투자를 받아 시행한 연구는 5편 (13.5%)으로 조사되었다. 이는 소아 대상 임상연구의 제약사 투자가 적다는 점이 영향을 끼친 것으로 보여진다. 지역별로 살펴보면 연구책임기관 중 연구를 많이 등록한 상위 6개의 기관 중 한 곳을 제외한 나머지 모두 서울에 있었으며, 총 23개의 연구책임기관 중 12곳이 서울특별시에 위치하고 있어 서울에 많이 치중되어 있고 지역별 불균형이 있음을 확인 할 수 있었다. 한방 기관만을 살펴보면 총 23개의 연구책임기관 중 대전대둔산한방병원, 부산대학교한방병원 2곳으로 조사되었다. 이는 전체 연구책임기관 중 8.7%에 해당하는 비율로, 한방 의료기관의 소아청소년 대상 중재연구 등록이 저조함을 알 수 있다.
소아는 성인의 보호가 필요한 취약한 대상이고, 의사결정의 자율성이 떨어지기 때문에 소아를 대상으로 하는 임상시험의 윤리적 고려 사항은 성인 대상 시험보다 복잡하다22). 2013년 식품의약품안전청에서 배포된 소아를 대상으로 하는 임상시험 평가 가이드라인에 따르면, 소아 연구대상자는 법적으로 정당한 동의를 할 수 없기 때문에 부모나 법적 대리인의 동의가 필요하며, 만 7세 이상부터는 소아 연구대상자에게도 짧은 문장의 설명문을 제공하여 동의를 받는 것이 권장된다23). 본 연구에서 동의 여부나 형태를 조사한 결과 명시되지 않음이 17편으로 가장 많았고, 부모나 법정대리인의 동의만 받은 경우가 9편 (24.3%), 소아의 연령에 따라 부모와 소아 모두에게 받거나 부모나 법정대리인의 동의만 받은 경우가 7편 (18.9%)으로 그 다음으로 많았다. 부모와 소아 모두에게서 동의를 받은 연구는 2편 (5.4%), 소아의 동의만 받은 연구는 없었다. 동의여부는 임상시험의 윤리적인 측면에서 중요한 사항임에도 불구하고 명시되지 않은 연구가 17편 (45.9%)으로 많은 비중을 차지하고 있다는 점에서 임상연구를 등록함에 있어 이 부분이 명확히 명시될 필요가 있어 보인다. 또한 만 7세 이상의 소아가 포함된 연구이지만 부모의 동의만 받은 연구는 4편인 것으로 조사되어, 만 7세 이상의 아동에게도 동의를 받는 것이 더욱 권장될 필요가 있다 생각된다.
국내 소아를 대상으로 하는 임상시험 평가 가이드라인에 따르면 보상 및 금전적 대가 지급은 소아 임상시험의 내용 중 언급이 되어야 한다고 명시되어 있다23). 소아 중재연구 참여자에 대한 보상이 어떻게 이루어지고 있는지 확인하고자 분석을 시도하였으나 보상에 관해 언급한 연구는 없었다. 이는 CRIS에서 필수 기재사항이 아니기 때문이라 사료된다. 임상시험 등록의 의의 중 하나가 일반인들에 대한 정보공개를 통해 임상시험에 참여할 수 있는 기회를 제공하는 것이기 때문에1), 향후 보상에 관한 내용도 CRIS에 등록될 필요가 있을 것으로 보인다.
소아 임상연구 시행 시 안전성을 조사하고 위험성을 최소화하여야 한다. 위험성은 최대한 광범위하게 평가되어야 하며, 모든 잠재적 위험성을 자세히 조사하여 소아 연구대상자는 연구에 참여한 결과로서 장해를 입어서는 안 된다24). 본 연구에서 안전성 조사 여부에 따라 분류한 결과, 안전성을 조사한 연구는 총 17편 (49.5%)으로 조사하지 않은 연구 (54.0%)보다 적은 것으로 나타나 안전성에 대한 조사가 미흡함을 알 수 있었다.
전반적으로, 국내 소아청소년 대상 중재연구는 규제 및 인센티브의 부재 등으로 다른 나라에 비해 부족한 상황이며, 국내 전체 임상 중재연구 중에서도 2-6%만을 차지하여 소아청소년 대상 중재연구가 매우 저조함을 알 수 있었다. 이에 소아청소년 대상 중재연구의 활성화를 위한 방안이 마련되어야 할 것으로 보인다. 또한 국제 사회의 흐름에 맞게 국내 또한 첫 연구대상자 모집 전 임상연구 등록이 의무화되고 소아 임상연구의 윤리적인 측면도 더욱 강화되어야 할 것으로 보여진다.
소아청소년 대상 한의 중재연구 현황만을 살펴보면, 한의 중재연구는 37편 중 3편으로 매우 부족하였고, 연구 책임기관 23곳 중 한방 의료기관이나 연구기관은 단 2곳으로 상대적으로 한의계에서 소아청소년 대상 중재연구가 아직까지는 많이 이루어지지 않고 있음을 알 수 있었다. 이에 한방 소아과 영역에서 향후 다양한 질환에 대한 다양한 한의 중재 연구를 시행하는 것이 필요하다 생각된다.
본 연구는 CRIS만을 이용하여 검색하였기 때문에 국내에서 시행되는 모든 소아청소년 대상 중재연구를 다루지는 못했다는 한계가 있다. 또한, CRIS에 등록된 정보를 통해 소아청소년 대상 임상 중재연구의 등록 현황 및 동향을 파악하는 연구로, 등록된 임상연구 개별의 현재 수행 상황을 정확하게 파악하지 못하는 한계가 있다. 따라서 향후 CRIS에 등록된 소아 임상연구가 어떻게 수행되고 있으며 진행되고 있는지에 관한 연구도 이뤄져야 할 것으로 보인다. 하지만 이러한 한계점에도 불구하고 향후 한방소아과 영역에서 소아청소년 대상 중재연구를 시행하는 데 있어 기초자료로서 도움을 줄 수 있을 것이라 사료된다.
Ⅴ. Conclusion
본 연구는 2018년 5월부터 2018년 10월까지 CRIS 등록부에 등록된 총 37편의 소아청소년 대상 중재연구를 정리, 분석하였다. 결과는 다음과 같다.
1. 연도별로 분석한 결과 2016년에 11편으로 가장 많이 등록되었으며 평균 등록된 연구는 4.7편이었다. 연도별 전체 중재연구 중 소아청소년 대상중재연구 (치료목적 외 포함)의 비중은 2-6% 정도로 저조함을 알 수 있었다.
2. 중재종류별로 분석한 결과 의약품 13편 (35.1%), 의료기구 7편 (18.9%)으로 가장 많았으며 이 외 두 가지 이상의 중재가 혼합되어 있는 경우, 시술/수술, 식이보충제, 행동요인 등이 중재로 사용되었다. 한의 중재가 포함된 연구는 총 3편으로 상대적으로 한의 중재가 부족함을 알 수 있었다. 사용된 한의 중재로는 본초추출물, 한약 엑스제 및 침 치료, 한약 입욕제가 있다. 향후 다양한 한의중재연구가 시행되어야 할 것으로 보인다.
3. 연구대상질환별로 분석한 결과 신경계통 질환 6편 (16.2%), 피부 및 피부 밑 조직 질환 5편 (13.5%), 근육골격계통 및 결합조직 질환 4편 (10.8%) 이었고, 개별 질환으로는 뇌성마비 6편, 아토피 피부염 3편 순이었다. 연구대상질환에 관계없이 수술 중이나 후에 중재가 시행된 경우는 12편으순로, 수술적 상황과 동반된 연구가 많이 시행됨을 알 수 있었다.
4. 동의 여부와 형태에 따라 분석한 결과, 동의 여부가 언급되지 않은 연구가 17편 (45.9%)으로 가장 많았으며, 부모나 법정대리인의 동의만 받은 경우가 9편 (24.3%), 부모와 소아 모두 또는 부모나 법정대리인의 동의만 받은 경우가 7편 (18.9%), 부모와 소아 모두에게서 동의를 받은 연구는 2편 (5.4%), 동의는 받았지만 누구에게서 받았는지 명시되지 않은 연구가 2편 (5.4%)으로 그 뒤를 따랐으며 소아의 동의만 받은 연구는 없었다.
5. 안전성 조사 여부에 따라 분류한 결과, 안전성을 조사한 연구는 총 17편 (49.5%)으로 조사하지 않은 연구 20편 (54.0%)보다 적은 것으로 나타나 안전성에 대한 조사가 미흡한 것으로 조사되었고, 향후 개선이 요구된다.
References
- Park HY. Primary registry of the WHO international clinical trial registry platform: Clinical Research Information Service (CRIS). J Korean Med Assoc. 2011; 54(1):92-7. https://doi.org/10.5124/jkma.2011.54.1.92
- Grimes DA, Schulz KF. An overview of clinical research: the lay of the land. Lancet. 2002;359(9300):57-61. https://doi.org/10.1016/S0140-6736(02)07283-5
- Thiese MS. Observational and interventional study design types; an overview. Biochem Med. 2014;24(2): 199-210. https://doi.org/10.11613/BM.2014.022
- Roberts R, Rodriguez W, Murphy D, Crescenzi T. Pediatric drug labeling: improving the safety and efficacy of pediatric therapies. JAMA. 2003;290(7):905-11. https://doi.org/10.1001/jama.290.7.905
- Chung EH. Clinical implication of adverse drug reaction surveillance in children. Allergy Asthma Respir Dis. 2016;4(5):309-10. https://doi.org/10.4168/aard.2016.4.5.309
- Steinbrook R. Testing medications in children. N Engl J Med. 2002;347(18):1462-70. https://doi.org/10.1056/NEJMhpr021646
- Caldwell PH, Murphy SB, Butow PN, Craig JC. Clinical trials in children. Lancet. 2004;364(9436):803-11. https://doi.org/10.1016/S0140-6736(04)16942-0
- Jung HJ, Park JE, Choi SM. Current status of institutional review boards and approvals of clinical research in oriental medical hospitals in Korea: a survey. J Korean Orient Med. 2010;31(1):122-9.
- Han JK, Kim YH. Health care utilization of pediatrics outpatients in the oriental hospital. J Pediatr Korean Med. 2001;15(2):209-20.
- Park YJ, Lee SJ, Yoon JY, Myoung SM. A survey on parent's recognition and utilization patterns of oriental medical care of preschool students in Seong-Dong district. J Pediatr Korean Med. 2011;25(1):90-110. https://doi.org/10.7778/jpkm.2011.25.1.090
- Lee JH, Lee EJ, Lee BR, Chang GT. Review of clinical research about herbal medicine treatment on recurrent respiratory tract infection in children. J Pediatr Korean Med. 2016;30(2):82-95. https://doi.org/10.7778/jpkm.2016.30.2.082
- Shin HJ, Lee BR, Lee JH, Chang GT. Review of clinical researches for herbal medicine treatment on nocturnal enuresis in children. J Pediatr Korean Med. 2018; 32(2):43-63. https://doi.org/10.7778/JPKM.2018.32.2.043
- Choi EY, Chang GT, Kim JH. Clinical trial study for childhood myopia in traditional Chinese medical journals. J Pediatr Korean Med. 2006;20(1):207-18.
- Bang MR, Kim JH, Min SY. The trends in foreign clinical trials for pediatric asthma in complementary and alternative medicine. J Pediatr Korean Med. 2015; 29(3):1-11. https://doi.org/10.7778/jpkm.2015.29.3.001
- Kim KR, Han JK, Kim YH. Review of Korean clinical studies on treatment for childhood obesity. J Pediatr Korean Med. 2016;30(3):108-20. https://doi.org/10.7778/jpkm.2016.30.3.108
- Yang DH, Park JK, Sung HK, Sung SH. Trend analysis of clinical studies published in the Journal of Pediatrics of Korean Medicine. J Pediatr Korean Med. 2018; 32(4):141-62. https://doi.org/10.7778/JPKM.2018.32.4.141
- Sammons H, Starkey E. Ethical issues of clinical trials in children. Paediatr Child Health. 2012;22(2):47-50. https://doi.org/10.1016/j.paed.2011.04.011
- Dickey M, Clark P. Changing the outcomes of pediatric drug trials: APNs making a difference. J Pediatr Health Care. 2013;27(3):222-5. https://doi.org/10.1016/j.pedhc.2013.01.005
- Park SY. Clinical trial regulation and status in US, EU, Japan and Korea for pediatric patients. Seoul, The Graduate School, Sungkyunkwan Univ. 2017.
- Chan L, Heinemann AW. Clinical trial registration: The time has come…. Arch Phys Med Rehabil. 2015; 96(12):2093. https://doi.org/10.1016/j.apmr.2015.09.005
- Mahan VL. Clinical trial phases. Int J Clin Med. 2014; 5(21):1374-83. https://doi.org/10.4236/ijcm.2014.521175
- Kelly B, Mackay-Lyons MJ. Ethics of involving children in health-related research: applying a decision-making framework to a clinical trial. Physiother Can. 2010;62(4): 338-46. https://doi.org/10.3138/physio.62.4.338
- Korea Food & Drug Administration. Guidelines for clinical trial evaluation in children [press release]. 2013.
- Oh MH. Ethical considerations for clinical trials performed in children. Korean J Pediatrics. 2009;52(1):1-5. https://doi.org/10.3345/kjp.2009.52.1.1